Gastrin-I(胃泌素)的作用機(jī)理及在類器官培養(yǎng)中的應(yīng)用_abio生物試劑品牌網(wǎng)
一、 Gastrin-I 的作用機(jī)理
Gastrin-I(胃泌素,AbMole,M9320)是一種多肽類生物活性分子,Gastrin-I通過與CCK2R結(jié)合,激活細(xì)胞內(nèi)信號(hào)通路,如提高細(xì)胞內(nèi)Ca 2+濃度、促進(jìn)磷酸肌醇生成和蛋白激酶C激活。此外,Gastrin-I還參與胃上皮細(xì)胞的增殖和分化過程,刺激胃泌酸腺區(qū)黏膜和十二指腸黏膜的DNA、RNA及蛋白質(zhì)合成,促進(jìn)黏膜細(xì)胞的生長(zhǎng)與增殖。
二、 Gastrin-I 用于類器官的培養(yǎng)
在胃類器官的培養(yǎng)過程中, Gastrin-I(胃泌素,AbMole,M9320)是培養(yǎng)基中的重要組分。研究表明,Gastrin-I能夠通過其受體激活下游信號(hào)通路,從而促進(jìn)胃上皮細(xì)胞的增殖和分化。例如,在一項(xiàng)研究中,Gastrin-I被添加到3D胃類器官的培養(yǎng)基中,濃度為1 nM,與其他生長(zhǎng)因子如表皮生長(zhǎng)因子(EGF)和成纖維細(xì)胞生長(zhǎng)因子10(FGF10)協(xié)同作用,顯著提高了類器官的形成效率和生長(zhǎng)速度 [1]。這種培養(yǎng)體系不僅能夠模擬胃組織的生理結(jié)構(gòu),還為研究胃腸道疾病提供了理想的模型 [1]。

 圖 1. 胃和腸道類器官的構(gòu)建
[2]
圖 1. 胃和腸道類器官的構(gòu)建
[2]
在小腸和結(jié)腸類器官培養(yǎng)中,Gastrin-I 同樣具有重要意義 Gastrin-I(胃泌素,AbMole,M9320)能夠促進(jìn)結(jié)腸上皮細(xì)胞的增殖和分化,維持結(jié)腸類器官的穩(wěn)定性和功能性。在結(jié)腸類器官的培養(yǎng)基中,Gastrin-I通常與TGF-β抑制劑如 A 83-01(AbMole,M5037 )、 LY2157299(AbMole,M1980)和p38MAPK抑制劑如 SB202190(AbMole,M2062)協(xié)同作用,以支持結(jié)腸干細(xì)胞的擴(kuò)增和分化 [3]。此外,Gastrin-I在小腸類器官的代謝功能中也具有重要作用,它能夠調(diào)節(jié)小腸上皮細(xì)胞的吸收功能,促進(jìn)營(yíng)養(yǎng)物質(zhì)的吸收和轉(zhuǎn)運(yùn)。這種調(diào)節(jié)作用對(duì)于維持小腸類器官的生理功能和穩(wěn)定性至關(guān)重要 [3]。 2014年,AbMole的兩款抑制劑分別被西班牙國(guó)家心血管研究中心和美國(guó)哥倫比亞大學(xué)用于動(dòng)物體內(nèi)實(shí)驗(yàn),相關(guān)科研成果發(fā)表于頂刊 Nature 和 Nature Medicine。
Gastrin-I(胃泌素,AbMole,M9320)在肝臟類器官培養(yǎng)中也是必不可少的成分之一。研究表明,Gastrin-I能夠通過激活下游信號(hào)通路,從而促進(jìn)肝細(xì)胞的增殖和分化。在肝臟類器官的培養(yǎng)基中,Gastrin-I通常與其他生長(zhǎng)因子如 EGF(AbMole,M10016)、 FGF10(AbMole,M10353)和 HGF(AbMole,M10352)協(xié)同作用,以支持肝臟干細(xì)胞的擴(kuò)增和分化。例如,一項(xiàng)研究中提到,在肝臟類器官的培養(yǎng)基中添加10 nM的重組人Gastrin-I,能夠顯著提高類器官的形成效率和生長(zhǎng)速度 [4]。
Gastrin-I(胃泌素,AbMole,M9320)還被廣泛用于多種腫瘤類器官的培養(yǎng),包括胃癌、結(jié)腸癌、胰腺癌和肝癌等。為腫瘤類器官在疾病研究和藥物篩選中的應(yīng)用提供了重要的支持。
三、 范例詳解 上海交通大學(xué)、吉林大學(xué)的研究團(tuán)隊(duì)探索了胰腺導(dǎo)管腺癌(PDAC)在Gemcitabine耐藥性發(fā)展過程中的動(dòng)態(tài)表觀遺傳學(xué)變化,特別是超級(jí)增強(qiáng)子及其調(diào)控效應(yīng)。研究使用了Gemcitabine耐藥(Gem-R)的PDAC細(xì)胞系,并構(gòu)建了類器官模型。實(shí)驗(yàn)人員還進(jìn)行了高通量的表觀基因組、增強(qiáng)子連接組和轉(zhuǎn)錄組分析。研究發(fā)現(xiàn),在從Gemcitabine敏感到耐藥的PDAC細(xì)胞轉(zhuǎn)變過程中,表觀遺傳景觀和基因組結(jié)構(gòu)發(fā)生了顯著變化。特別是超級(jí)增強(qiáng)子的激活狀態(tài)表現(xiàn)出極大的可塑性,許多順式元件在耐藥細(xì)胞中被去激活。此外,研究還確定了NDRG1超級(jí)增強(qiáng)子(NDRG1-SE)是Gemcitabine耐藥中一個(gè)關(guān)鍵的調(diào)控因子,NDRG1-SE的關(guān)閉誘導(dǎo)了WNT/β-catenin信號(hào)通路的激活,從而賦予了細(xì)胞對(duì)Gemcitabine的耐藥 [5]。在上述研究中,實(shí)驗(yàn)人員使用了由AbMole提供的多個(gè)產(chǎn)品: Gastrin I(胃泌素,AbMole,M9320 )、 Forskolin(AbMole,M2191 )、 Y-27632(AbMole,M1817 )、 A83-01(AbMole,M5037 )、 Dexamethasone(AbMole,M2176 )、 Prostaglandin E2(AbMole,M5929 )、 Nicotinamide(AbMole,M4896),并用于PDAC類器官的培養(yǎng) [5]。
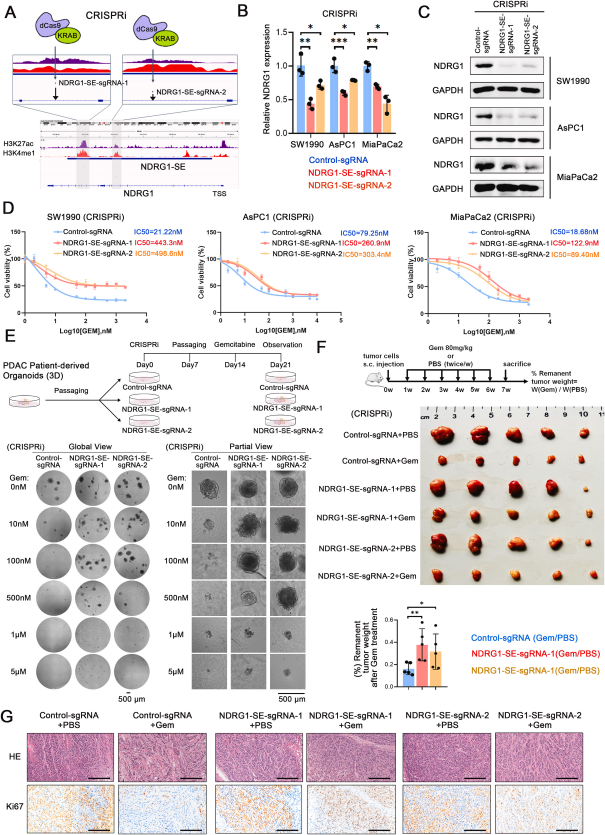
 圖 2. Induction of Chemoresistance to Gemcitabine by NDRG1 Super-Enhancer Deactivation
[5]
圖 2. Induction of Chemoresistance to Gemcitabine by NDRG1 Super-Enhancer Deactivation
[5]
AbMole是ChemBridge中國(guó)區(qū)官方指定合作伙伴。


參考文獻(xiàn)及鳴謝
[1] Jayati Chakrabarti, Yana Zavros, Chapter 2 - Generation and use of gastric organoids for the study of Helicobacter pylori pathogenesis, in: J.R. Spence (Ed.), Methods in Cell Biology, Academic Press2020, pp. 23-46.
[2] C. Günther, B. Winner, M. F. Neurath, et al., Organoids in gastrointestinal diseases: from experimental models to clinical translation, Gut 71(9) (2022) 1892-1908.
[3] Antonio Barbáchano, Asunción Fernández-Barral, PIlar Bustamante-Madrid, et al., Organoids and Colorectal Cancer, 13(11) (2021) 2657.
[4] E. De Crignis, T. HossAIn, S. Romal, et al., Application of human liver organoids as a patient-derived primary model for HBV infection and related hepatocellular carcinoma, eLife 10 (2021).
[5] Dianhui Wei, Lili Yuan, Xiaoli Xu, et al., Exploring epigenetic dynamics unveils a super-enhancer-mediated NDRG1-β-catenin axis in modulating gemcitabine resistance in pancreatic cancer, Cancer letters 605 (2024) 217284.
本站“ABIO生物試劑品牌網(wǎng)”圖片文字來自互聯(lián)網(wǎng)
如果有侵權(quán)請(qǐng)聯(lián)系微信: nanhu9181 處理,感謝~